Законы какой теории составляют фундамент изучения строения вещества
Обновлено: 17.05.2024
Законы какой теории составляют фундамент изучения строения вещества
Повторите основные положения темы «Основные понятия химии» и решите предложенные задачи. Используйте материалы уроков химии 8 класса №№6-17.
Видео YouTube
Основные положения
1. Вещество (простое и сложное) – это любая совокупность атомов и молекул, находящаяся в определённом агрегатном состоянии.
Превращения веществ, сопровождающиеся изменением их состава и (или) строения, называется химическими реакциями .
2. Структурные единицы вещества:
· Атом – наименьшая элекронейтральная частица химического элемента и простого вещества, обладающая всеми его химическими свойствами и далее физически и химически неделимая.
· Молекула – наименьшая электронейтральная частица вещества, обладающая всеми его химическими свойствами, физически неделимая, но делимая химически.
3. Химический элемент – это вид атомов с определённым зарядом ядра.
4. Состав атома :
5. Состав атомного ядра :
· В состав ядра входят элементарные частицы ( нуклоны ) –
протоны ( 1 1 p ) и нейтроны ( 1 0 n ).
· Т.к. практически вся масса атома сосредоточена в ядре и mp ≈ mn ≈ 1 а.е.м , то округлённое значение Ar химического элемента равно общему числу нуклонов в ядре.
(А – массовое число, округлённое значение А r ; N – число нейтронов в ядре; Z – заряд ядра, равный числу протонов)
6. Общее число электронов в электронной оболочке атома N ē равно числу протонов в ядре и порядковому номеру химического элемента
7. Изотопы – разновидность атомов одного и того же химического элемента, отличающиеся друг от друга только своей массой.
· Обозначение изотопов: слева от символа элемента указывают массовое число (вверху) и порядковый номер элемента (внизу)
· Почему у изотопов разная масса?
Задание: Определите атомный состав изотопов хлора: 35 17 Cl и 37 17 Cl ?
· Изотопы имеют разную массу из-за различного числа нейтронов в их ядрах.
8. В природе химические элементы существуют в виде смесей изотопов.
Изотопный состав одного и того же химического элемента выражают в атомных долях (ωат.) , которые указывают какую часть составляет число атомов данного изотопа от общего числа атомов всех изотопов данного элемента, принятого за единицу или 100%.
9. В таблице Менделеева приведены средние значения относительных атомных масс химических элементов с учётом их изотопного состава. Поэтому Ar , указанные в таблице являются дробными.
Ar ср = ω ат.(1) ∙ Ar (1) + … + ω ат.( n ) ∙ Ar ( n )
Ar ср ( Cl ) = 0,754 ∙ 35 + 0,246 ∙ 37 = 35,453
10. Задача для решения:
№1. Определите относительную атомную массу бора, если известно, что молярная доля изотопа 10 В составляет – 19,6 %, а изотопа 11 В – 80,4 %.
11. Массы атомов и молекул очень малы. В настоящее время в физике и химии принята единая система измерения.
1 а.е.м. = m (а.е.м.) = 1/12 m ( 12 C ) = 1,66057 ∙ 10 -27 кг = 1,66057 ∙ 10 -24 г .
Абсолютные массы некоторых атомов:
m ( C ) = 1,99268 ∙ 10 -23 г
m ( H ) = 1,67375 ∙ 10 -24 г
m ( O ) = 2,656812 ∙ 10 -23 г
Ar – показывает, во сколько раз данный атом тяжелее 1/12 части атома 12 С.
М r – показывает, во сколько раз данная молекула тяжелее 1/12 части атома 12 С.
12. Связь между абсолютной и относительной массами атома или молекулы:
m (атома) = Ar ∙ 1,66 ∙ 10 -27 кг
m (молекулы) = Mr ∙ 1,66 ∙ 10 -27 кг
13. Число атомов и молекул в обычных образцах веществ очень велико, поэтому при характеристике количества вещества используют единицу измерения – моль .
· Моль (ν) – единица количества вещества, которое содержит столько же частиц (молекул, атомов, ионов, электронов), сколько атомов содержится в 12 г изотопа 12 C
· Масса 1 атома 12 C равна 12 а.е.м., поэтому число атомов в 12 г изотопа 12 C равно:
NA = 12 г / 12 ∙ 1,66057 ∙ 10 -24 г = 6,0221 ∙ 10 23
· Физическая величина NA называется постоянной Авогадро (число Авогадро) и имеет размерность [ NA ] = моль -1 .
14. Основные формулы:
M = Mr = ρ ∙ Vm ( ρ – плотность; Vm – объём при н.у.)
Задачи для самостоятельного решения
№1. Вычислите число атомов азота в 100г карбоната аммония, содержащего 10% неазотистых примесей.
№2. При нормальных условиях 12 л газовой смеси, состоящей из аммиака и углекислого газа, имеют массу 18 г. Сколько литров каждого из газов содержит смесь?
Вещество и его свойства. Атомно-молекулярное учение.
Иначе химические явления называют химическими реакциями .
Каждое вещество обладает строго определёнными свойствами.
Свойства веществ – признаки, позволяющие отличить одни вещества от других, или установить сходство между ними.
Физические свойства :
m - масса, V - объём, ρ - плотность.
Масса может быть выражена в граммах, объем в миллилитрах (если это жидкость) или литрах (если это газ).
1 мл = 1 см3, 1 л = 1 дм3, 1000 л = 1 м3
Поэтому плотность измеряют в г/мл, г/см3 (если это жидкость), или в г/л, г/дм3 (если это газ).
Если принять V = 1, то плотность - это масса единичного объёма вещества.
Химические свойства - это те химические реакции, в которые вступает данное вещество.
Так же можно сказать, что химические свойства - это те химические реакции, которые характеризуют группу веществ (класс веществ). Например, мы будем в дальнейшем изучать свойства воды, свойства класса оксидов, свойства класса алканов и т.д.
ООсновы атомно – молекулярного учения
Идея о том, что вещества состоят из мельчайших частиц возникла в Древней Греции в философских учениях Левкиппа и его ученика Демокрита. Эти частицы они назвали атомами (неделимые).
Существование атомов было доказано эмпирическим путём в конце 16 – начале 17 века Джоном Дальтоном и М. В. Ломоносовым. Ими же были заложены основы атомно – молекулярного учения .
В настоящее время, в связи с открытием делимости атома и появлением теории химической связи, основные положения атомно – молекулярного учения существенно изменились. Его суть можно свести к ряду важных положений, которые необходимо запомнить.
Все вещества, существующие в природе, представляют собой совокупность очень большого числа частиц (атомов, молекул или ионов). В зависимости от типа частиц все вещества условно подразделяют на две группы: вещества молекулярного строения и вещества немолекулярного строения (атомного или ионного).
Вещества молекулярного строения – вещества, основной структурной единицей которых является молекула.
Вещества немолекулярного строения – вещества, основными структурными единицами которых являются атомы или ионы.
Частицы, из которых состоит данное вещество, взаимодействуют между собой посредством электромагнитных (кулоновских) сил и находятся в постоянном движении. Движение частиц ограничено силами взаимодействия между ними.Каждое вещество, в зависимости от условий (температуры, давления) может находиться в определённом агрегатном состоянии.
В твёрдом агрегатном состоянии вещества, составляющие его частицы находятся относительно упорядоченно (кристаллическое состояние), их кинетическая энергия (энергия движения) существенно меньше чем потенциальная (энергия покоя). В газообразном состоянии, частицы свободно движутся в предоставленном им объёме и их кинетическая энергия существенно выше чем потенциальная.
В жидкости же потенциальная энергия частиц примерно равна их кинетической энергии. Это связано с тем, что часть частиц жидкости находится относительно упорядоченно в составе так называемых кластеров (англ. cluster — скопление). Другие же частицы свободно перемещаются по объёму жидкости. Чем ниже температура жидкости, тем больше в ней кластеров и наоборот.
Рис. Кластеры воды, где число молекул 20-220 Рис. Кластеры воды, где число молекул 20-220Следует отметить, что существуют еще два дополнительные "состояния". Это жидкокристаллическое состояние и состояние плазмы .
Цитоплазматическая мембрана клетки - типичный пример жидкого кристалла. Молекулы фосфолипидов в биологической мембране относительно упорядоченно распределяются в двух слоях, но при этом могут в пределах слоя свободно перемещаться, а также "перескакивать" из одного слоя в другой.
Жидкие кристаллы имеют широкое применение в технике (напр., ЖК-мониторы компьютеров).
Плазма (от греч. πλάσμα «вылепленное», «оформленное») — ионизованный газ.
Плазма в своём составе содержит свободные электроны, катионы (положительно заряженные ионы) и анионы (отрицательно заряженные ионы).
Так как плазма содержит заряженные частицы, то она проводит электрический ток и на неё можно воздействовать внешним магнитным полем. Различают низкотемпературную и высокотемпературную плазму.
Изучает свойства плазмы наука физика.
Вещество из одного агрегатного состояния может переходить в другие агрегатные состояния при изменении внешних условий - температуры (T) и давления (P). Такие переходы принято называть фазовыми переходами .
Так, при повышении температуры, твердое вещество превращается в жидкость, а жидкость при ещё большей температуре превращается в газ. Дальнейшее повышение температуры переводит газ в плазму. При таких переходах вещество в другие вещества не превращается. Напомним, что такие явления мы называем физическими. Поэтому фазовые переходы - это физические явления.
При понижении температуры происходят обратные фазовые переходы - газ превращается в жидкость, а жидкость переходит в твердое состояние.
Атомная теория строения вещества от античности до современности
Само слово "атом" имеет греческое происхождение и в буквальном переводе означает – неделимый. Считается, что саму идею о том, что гладкая и на беглый взгляд непрерывная материя в реальности состоит из огромного количества микроскопических (а поэтому и невидимых) частиц, предложил древнегреческий философ Демокрит, который блистал своим умом в V веке до нашей эры.
К сожалению, труды самого философа-мыслителя до наших дней не дошли, и о его работах мы судим в основном на основании авторов других работ, которые цитировали выдержки его трудов. И в основном ориентируемся на Аристотеля.
Простая логика Демокрита
Если попытаться адаптировать логику философа к современным реалиям, то получится вот такая цепочка рассуждений:
Возьмем абсолютно любой объект (который попадется вам под руку) и начнем его разрезать самым острым в мире ножом. Затем берем одну из получившихся половинок и ее так же разрезаем пополам. И продолжаем этот процесс снова и снова.
Так вот, продолжая такой процесс деления, мы с вами обязательно дойдем до того момента, что получим столь малую частицу материи, которую будет уже невозможно поделить на две половинки. Это и будет искомый и неделимый атом материи.
По рассуждениям Демокрита, атомы являлись вечными, неделимыми и оставались неизменными постоянно. А все изменения во Вселенной происходили исключительно за счет изменений связей между атомами.
Вот так зародилась теория Атома.
Современные представления об атоме
На текущий момент от умозаключений древних философов осталось лишь одно название – «атом». Теперь практически каждый школьник знает, что атом сам состоит из множества так называемых фундаментальных частиц.
Но для того, чтобы все это понять, современным ученым пришлось провести огромное количество опытов. А древний философ мог положиться только на силу своего разума и в ходе рассуждений делал заключения относительно мироустройства.
И сама идея атомарного устройства мира была лишь философской вплоть до 19 века. Именно в это время началось формирование такой науки как химия. Именно химики первые установили, что в ходе реакций очень многие вещества разлагаются на более простые составные компоненты.
Например, вода (H2O) распадается на кислород и водород, а вот уже сам кислород и водород дальнейшему разложению (при химических реакциях) не подвергается.
Вещества, которые никак не изменялись в ходе химических реакций, получили название "химические элементы".
Помимо этого было установлено крайне важное обстоятельство. Оказывается, что во время протекания химической реакции количественное соотношение веществ в одной реакции остается неизменной.
Объяснил все эти моменты ученый Джон Дальтон. Так в 1808 году он опубликовал двухтомник "Новая система химической философии".
Если кратко, то в своих трудах он предложил принять тот факт, что каждому химическому элементу принадлежит уникальный атом. И в результате смешения именно этих уникальных атомов образуются все химические вещества в мире.
Возьмем ту же воду. По Дальтону вода состоит из единственного атома кислорода и пары атомов водорода.
Причем неважно, где бы вы ни взяли воду, она всегда будет состоять из одних и тех же элементов.
Так вот, как и для Демокрита, для Дальтона атомы - это абсолютно неделимые кирпичики мироздания. Но главная мысль трудов ученого 19 века в том, что каждому химическому элементу присущ особый атом, до сих пор является основополагающей для современной химии.
И это несмотря на то, что мы прекрасно знаем, что атом — это сложная конструкция из множества более мелких элементов.
Получается, что несмотря на прошедшие тысячелетия сама концепция атома не исчерпана и в начале 21 столетия.
Понравился материал? Тогда оцените его лайком, репостом и комментарием. Спасибо, что прочитали до конца.
Законы какой теории составляют фундамент изучения строения вещества

Основные положения
теории химического строения
Ключевые слова конспекта: Теория химического строения органических соединений. Валентность. Структурная формула. Простые (одинарные) связи. Кратные (двойные и тройные) связи. Изомеры. Изомерия. Взаимное влияние атомов в молекуле.
Содержание (быстрый переход): СкрытьПредпосылки создания теории химического строения
По мере накопления химических знаний учёные овладели умением не только выделять органические вещества из природных объектов, но и проводить реакции с участием таких соединений. Так накапливались знания о свойствах органических веществ, расширялись области их практического применения.
В начале XIX в. учёными-химиками были разработаны методы определения качественного и количественного состава органических веществ. Стало возможным получить ответ на вопрос, какие химические элементы входят в состав этих соединений и каково их соотношение. Однако учёные тогда ещё не могли объяснить, как атомы соединяются в молекулы, не могли записывать качественный и количественный состав веществ с помощью формул; химические реакции описывали словами. Выдающийся немецкий химик того времени Ф. Вёлер писал: «Органическая химия может сейчас кого угодно свести с ума. Она кажется мне дремучим лесом, полным удивительных вещей, безграничной чащей, из которой нельзя выбраться, куда не осмеливаешься проникнуть…»
К середине XIX в. возникла необходимость осмысления, объяснения и обобщения накопившихся данных в области органической химии, т. е. создания научной теории, которая позволила бы систематизировать и объяснять строение и свойства органических веществ.
В первой половине XIX в. учёными разных стран были предприняты попытки создания подобной теории. Одни основывались на сходстве качественного и количественного состава родственных органических веществ, другие — на общности химических свойств. Однако подобно тому, как первые попытки классификации химических элементов не превратились в научную теорию, а стали лишь предтечей открытия Д. И. Менделеевым периодического закона, так и ранние попытки систематизации знаний об органических веществах явились предпосылками создания теории химического строения органических соединений.
Первое положение теории химического строения.
Структурные формулы
Первую научную теорию строения органических соединений, которой химики всего мира придерживаются до сих пор, предложил выдающийся русский учёный А. М. Бутлеров. Основные идеи новой теории впервые были высказаны им в 1861 г. в докладе «О химическом строении вещества» на съезде естествоиспытателей и врачей в немецком городе Шпайере.
Основой теории Бутлерова является положение о химическом строении как определённой последовательности химических связей между атомами в молекулах в строгом соответствии с их валентностью. Рассмотрим основные положения теории химического строения.
Напомним, что валентность — это способность атомов химических элементов образовывать определённое число связей с другими атомами. Для соединений с ковалентными связями валентность равна числу общих электронных пар данного атома с соседними атомами.
Наглядно продемонстрировать валентность атомов в молекуле можно с помощью структурных формул. Структурная формула — это такое изображение молекулы, в котором каждая ковалентная химическая связь показана чёрточкой — валентным штрихом.

В органических соединениях углерод проявляет постоянную валентность, равную четырём. Например, структурная формула простейшего углеводорода метана СН4 имеет вид

Атомы углерода обладают уникальной способностью образовывать связи не только с атомами других элементов, но и друг с другом; при этом возникают различные цепи — линейные, разветвлённые, замкнутые:
Атомы углерода во всех приведённых примерах четырёхвалентны и образуют между собой и с атомами водорода простые, или одинарные, связи.

Но этим уникальные особенности атомов углерода как химического элемента не исчерпываются. Два атома могут быть связаны между собой и с другими атомами не только простыми, но и кратными, т. е. двойными или даже тройными, связями, например:
Теперь вам становится понятна одна из причин многообразия органических соединений. Она заключается в том, что атомы углерода способны образовывать между собой ковалентные химические связи (простые и кратные), соединяясь в цепи (неразветвлённые, разветвлённые, циклические).
Второе положение теории
химического строения. Изомерия

Чтобы описать свойства какого-либо органического вещества, например имеющего формулу C2H2О, недостаточно информации о качественном и количественном составе вещества. Необходимо знать, в каком порядке атомы соединены в молекуле. Подобно тому, как из одного и того же набора кубиков можно сложить домики разной «архитектуры», так и из двух атомов углерода, шести атомов водорода и одного атома кислорода можно без нарушения валентности «построить» различные молекулы:
Первое вещество — этиловый спирт и второе — диметиловый эфир имеют одинаковый состав, но их физические и химические свойства различны. Вы впервые встретились с очень распространённым в органической химии явлением — изомерией.
Вещества, имеющие одинаковый качественный и количественный элементный состав, но различное химическое строение, а следовательно, и различные свойства, называют изомерами. Явление существования изомеров называют изомерией.
А. М. Бутлеров не только впервые объяснил существование изомеров различием в химическом строении молекул, но и сумел предсказать существование изомеров для уже известных веществ, а затем и синтезировать их. В этом заключается выдающаяся предсказательная роль теории строения.
Таким образом, молекулярная формула отражает только качественный и количественный состав вещества. Информацию о химическом строении соединения несёт структурная формула, указывающая на порядок связи атомов в молекулах. Помимо полной структурной формулы наподобие тех, которые изображены выше, на практике чаще используют сокращённые структурные формулы, сворачивая близлежащие группы атомов, не записывая ненужные при этом валентные штрихи. Например, особенности строения этилового спирта и диметилового эфира вполне однозначно передают формулы:

Более детальную информацию о химическом строении вещества, в частности о взаимном расположении атомов в пространстве, дают объёмные модели молекул — модели Стюарта—Бриглеба.
Явление изомерии — ещё одна причина многообразия органических соединений.
Третье положение теории химического строения
Нетрудно догадаться, что этот «особенный» атом, в отличие от пяти остальных, не соединён с углеродом непосредственно, а связан с ним через атом кислорода. Следовательно, атом кислорода влияет на соседний с ним атом водорода, облегчая его замещение атомом натрия.
В молекуле диметилового эфира все атомы водорода связаны только с атомами углерода. Становится понятно, почему, в отличие от этилового спирта, диметиловый эфир не способен реагировать с металлическим натрием.
Теория химического строения, предложенная А. М. Бутлеровым, сыграла в органической химии такую же огромную роль, как периодический закон и периодическая система элементов Д. И. Менделеева в неорганической химии. Она позволила систематизировать все накопленные сведения об органических веществах и объяснить причины их многообразия. Но самое главное — теория строения сделала осмысленным и целенаправленным синтез новых органических веществ и изучение их химических свойств. Она настолько многогранна и динамична, что и сегодня является основополагающим учением не только органической, но и всей современной химии.
Основные выводы по теме конспекта:
- Научной основой органической химии является современная теория химического строения органических соединений. Некоторые положения этой теории:
- атомы в молекулах соединены друг с другом согласно их валентности, причём углерод в органических веществах всегда четырёхвалентен;
- свойства веществ зависят не только от их качественного и количественного состава, но и от их строения (химического, электронного и пространственного);
- атомы в молекулах влияют друг на друга.
- Химическим строением называют порядок расположения атомов в молекуле согласно их валентности.
- Химическое строение отображают с помощью химических формул: молекулярных и структурных (полных или сокращённых).
- Материальные модели, отражающие состав и пространственное строение молекул органических соединений, бывают двух видов: шаростержневые и объёмные.
- Причины многообразия органических веществ — это: способность атомов углерода соединяться друг с другом, образуя различные цепи (линейные, разветвлённые, циклические); способность атомов углерода образовывать связи различной кратности (одинарные, двойные, тройные); явление изомерии.
Конспект урока по химии «Основные положения теории химического строения». В учебных целях использованы цитаты из пособия «Химия. 10 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие:
Законы какой теории составляют фундамент изучения строения вещества

Современные представления о строении атома
Элемент ЕГЭ: 1.1 Современные представления о строении атома. 1.1.1 Строение электронных оболочек атомов элементов первых четырех периодов: s-, р- и d-элементы. Электронная конфигурация атома. Основное и возбуждённое состояние атомов.
Содержание (быстрый переход): СкрытьСовременные представления о строении атома

Атом – химически неделимая электронейтральная частица, которая состоит из положительно заряженного ядра и движущихся вокруг него отрицательно заряженных электронов.
Атомы не имеют заряда (нейтральны). Если атом присоединяет один или несколько электронов, он приобретает отрицательный заряд и превращается в анион. Если атом теряет один или несколько электронов, он приобретает положительный заряд и превращается в катион. Заряд иона указывают арабской цифрой и знаком после символа атома.
Состав ядра: А = Z + N, где А — массовое число; Z — протонное число (число протонов); N — число нейтронов.
Элементарные частицы
Порядковый номер элемента в периодической системе:
- Заряд ядра атома
- Число протонов в ядре атома
- Число электронов в атоме

Нуклиды – разновидности атомов с фиксированным массовым числом А, числом протонов Z и нейтронов N в ядре.

Основные положения квантовой теории строения атома:
- Дискретность энергии электрона
- Двойственная (корпускулярно-волновая) природа электрона
- Невозможность определения траектории электрона (принцип неопределенности)
Относительная атомная масса элемента (Ar)
Физическая величина, показывающая, во сколько раз средняя масса атомов данного элемента больше 1/12 части массы изотопа углерода 12 С.

Атомные орбитали
Орбиталь — пространство вокруг ядра, в котором нахождение электрона наиболее вероятно (вероятность более 90%)

Порядок заполнения орбиталей в основном состоянии
1) Принцип наименьшей энергии. Электроны занимают в первую очередь орбитали, имеющие наименьшую энергию.


2) Принцип Паули. На каждой орбитали могут находиться не более двух электронов, причём спины их противоположны.
Спин электрона — свойство электрона, характеризующее его способность взаимодействовать с магнитным полем. Может принимать два значения (положительное и отрицательное).

Последовательность заполнения орбиталей электронами в основном состоянии:
Энергетические уровни и подуровни

Элементы, у которых идет заполнение s-подуровня, называют s-элементами.
Элементы, у которых заполняется р-подуровень, называют р-элементами.
Элементы, у которых заполняется d-подуровень, называют d-элементами.
Элементы, у которых заполняется f-подуровень, называют f-элементами.
Распределение электронов в атоме по энергетическим уровням (электронным слоям) и подуровням
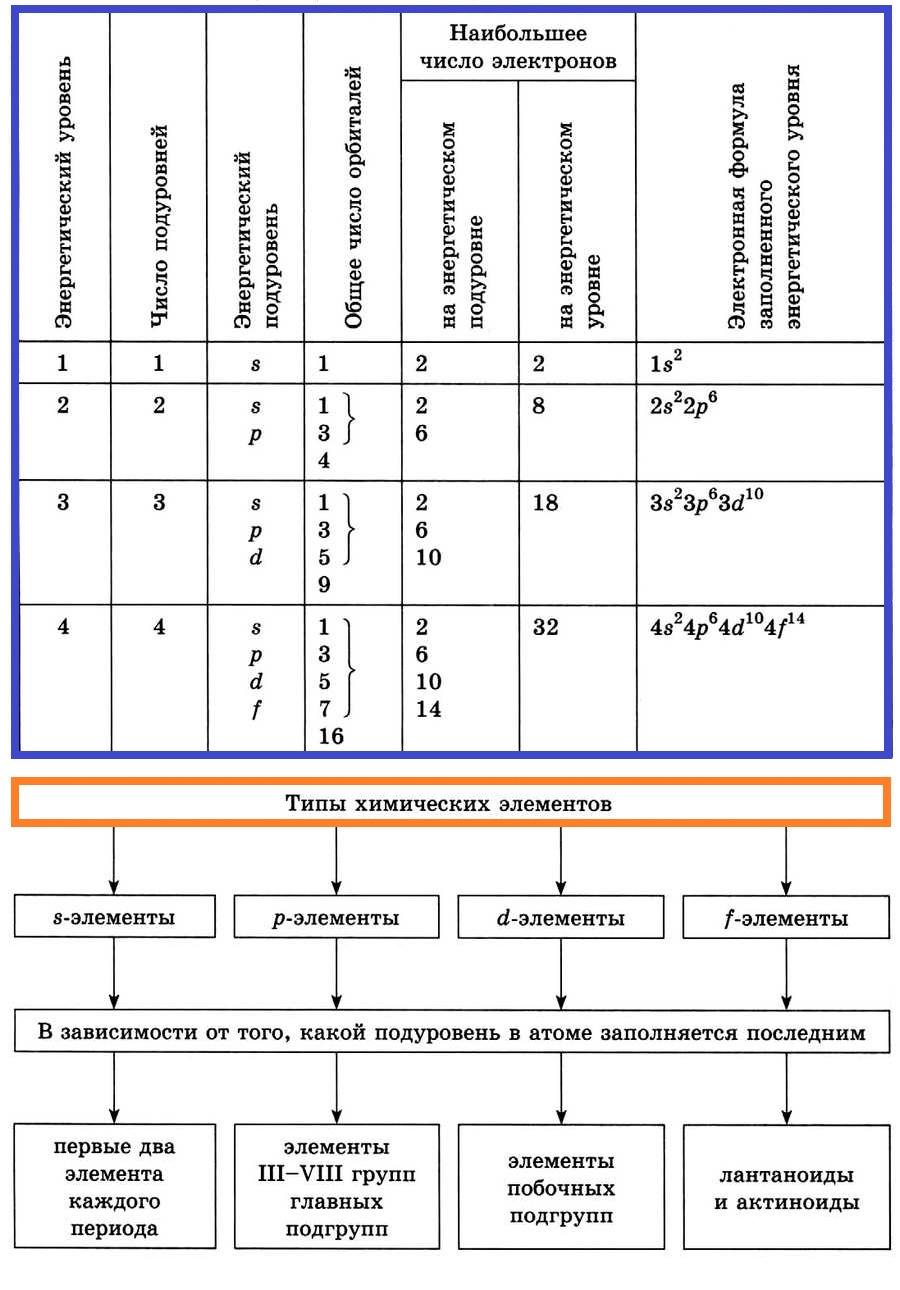
Электроны, относящиеся к последнему энергетическому уровню, называют внешними (валентными) электронами.
Строение электронных оболочек атомов первых четырёх периодов
Распределение электронов по орбиталям атома называют электронной конфигурацией атома, или электронной формулой.
Строение элементов первого периода

Строение элементов второго периода

Строение элементов третьего периода

Строение элементов четвёртого периода

Электронные конфигурации d 5 и d 10 обладают повышенной устойчивостью, поэтому в атомах хрома и меди наблюдается «перескок» электрона с 4s-подуровня на 3d-подуровень («провал электрона»).
Основное и возбуждённое состояние атомов
Наиболее устойчивое состояние атома, в котором энергия его электронной оболочки минимальна, называется основным состоянием атома. Любые другие состояния атома называют возбужденными состояниями.

Для возможности перехода атома в возбуждённое состояние необходимо выполнение одновременно двух условий:
- наличие спаренных электронов;
- наличие вакантных орбиталей.
Таблица «Современные представления о строении атома. Кратко»

(с) В учебных целях использованы цитаты из пособий: «Химия / Н. Э. Варавва, О. В. Мешкова. — Москва, Эксмо (ЕГЭ. Экспресс-подготовка)» и «Химия : Новый полный справочник для подготовки к ЕГЭ / Е.В. Савинкина. — Москва, Издательство АСТ».
Вы смотрели Справочник по химии «Современные представления о строении атома». Выберите дальнейшее действие:
Законы какой теории составляют фундамент изучения строения вещества


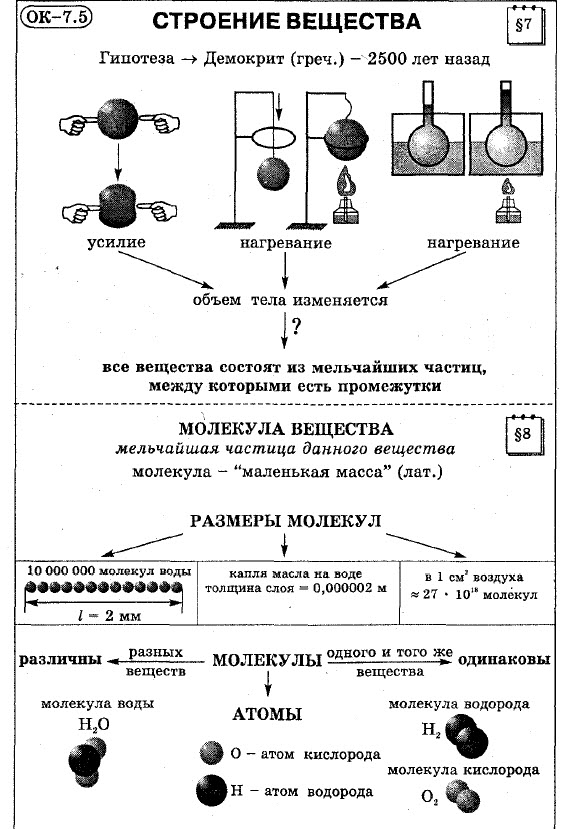
Строение вещества
Мельчайшей частицей вещества, которая определяет все свойства данного вещества, является молекула. Молекула состоит из атомов. Число атомов и их распределение в молекуле является различным. В природе существует немногим более сотни атомов различного вида. Элементы обобщены и расположены в периодической таблице химических элементов, им даны наименования, например, водород, азот, углерод.
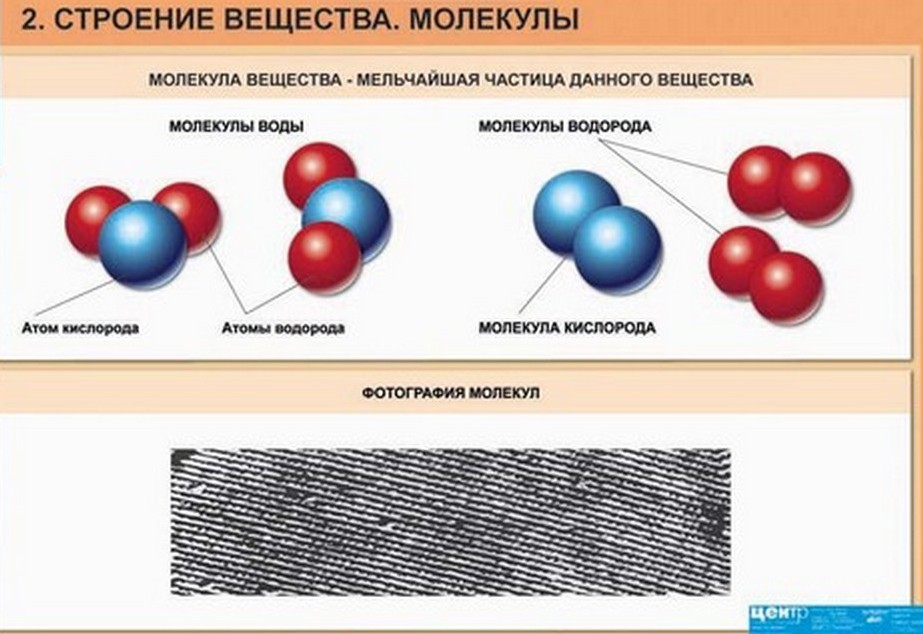
Движение частиц вещества называют тепловым движением.
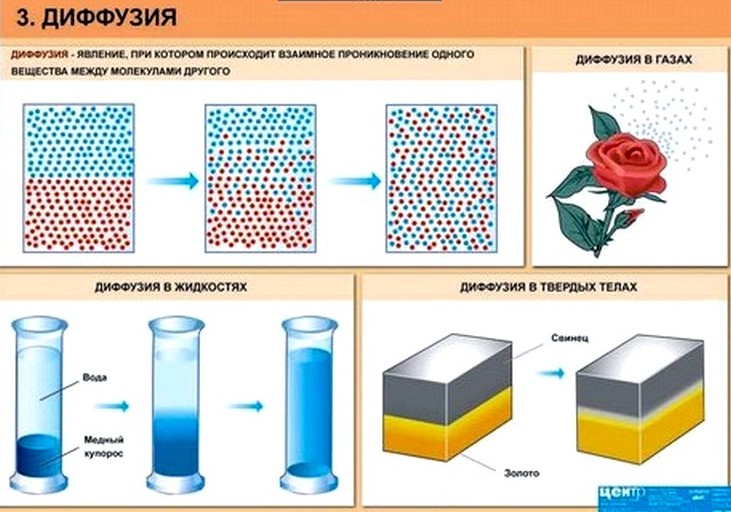
Броуновское движение — беспорядочное движение микроскопических видимых, плавающих в жидкости или газе частиц твёрдого вещества, вызываемое тепловым движением частиц жидкости или газа.
Взаимное проникновение частиц одного вещества в другое, обусловленное движением молекул, называют диффузией (от латинского «диффузио» — распространение, растекание).
Состояние вещества.
Вещества в природе встречаются в трёх состояниях:
Молекулы одного и того же вещества в различных состояниях не отличаются друг от друга. Различные свойства вещества во всех состояниях определяются тем, что его молекулы расположены иначе и движутся по-разному.
Каждому твёрдому телу характерна твёрдость. Твёрдость — способность тела сопротивляться воздействию другого тела. Твёрдость вещества выясняют, царапая его каким-либо другим веществом.
Существуют различные шкалы твёрдости. Одна из них составлена в 1811 году немецким минералогом Фридрихом Моосом. Она состоит из 10 уровней, самым мягким веществом в ней является тальк, а самым твёрдым — алмаз. Алмаз в 58 раз твёрже стоящего на втором месте по твёрдости минерала корунда, из которого изготавливают рубины и сапфиры.
Свойством тел, изготовленных из твёрдого вещества, является их деформация. Деформация — изменение формы или размера тела под воздействием другого тела.
Эластичностью называют возможность тела после деформации возвращать себе первоначальную форму. Пластилин является пластичным, ему легко придать любую форму, которая сохраняется.
Прочность — способность вещества сопротивляться разрушению. У каждого материала имеется свой предел прочности. Стекло нельзя гнуть, т.к. оно хрупкое. Очень прочными являются металлы.
Кристаллы — это твёрдые тела, в которых атомы расположены закономерно, упорядоченно, образуя кристаллическую решётку. Это лёд, соль, металлы, минералы и т.д.
Аморфные тела — тела, не имеющие строгой кристаллической решётки, бесформенные тела. («аморфный» происходит от греч. «аморфос» — бесформенный)
В отличие от кристаллов, стабильно-аморфные вещества не затвердевают с образованием кристаллических граней.
Структуры жидкостей и аморфных тел имеют много общего. По этой причине принято считать аморфные тела очень густыми, вязкими, застывшими жидкостями. Аморфные вещества могут находиться либо в стеклообразном состоянии при низких температурах, либо в состоянии расплава при высоких температурах. Аморфные тела обладают текучестью, хотя и значительно меньшей, чем жидкости. При повышении температуры текучесть аморфных тел увеличивается. Благодаря этому из капли нагретого стекла можно выдуть стеклянный сосуд.
Законы какой теории составляют фундамент изучения строения вещества
1824 г. – Вёлер синтезирует щавелевую кислоту,
1854 г. – Бертло синтезирует жиры,
1861г. – Бутлеров синтезирует один из углеводов.
Химики-органики не могли объяснить, почему:
- в органических соединениях углерод проявляет разную валентность - CH4 (IV); C2H6 (III); C6H6 (I)
- существуют вещества с разными свойствами, но с одинаковым составом молекулы – формуле C6H12O6 соответствует состав глюкозы и фруктозы.
- органических веществ десятки миллионов, а неорганических не достигает и 1 млн.

1 положение:
Атомы в молекулах соединены друг с другом в определённом порядке, согласно их валентностям ( C ( IV ), O ( II ), S ( II ), N ( III )), образуя прямые, разветвлённые и замкнутые цепи
Атомы углерода могут соединяться друг с другом одинарными, двойными и тройными связями: С ─ С, С=С, С ≡С
Атомная теория
Атомной теорией является такая теория, которая основана на гипотезе о том, что абсолютно все в природе и космосе состоит из очень мелких частиц, которые называются атомы. Они соединяются между собой под воздействием ядерных и электрических сила.

Появление атомной теории
Слово «атом» возникло в Древней Греции, и в переводе обозначает «неделимый».
Философ Древней Греции Демокрит первый предложил теорию о том, что все состоит из очень мелких частиц, которых очень много вокруг нас. Его теория гласила о том, что атомы вечны, неделимы и неизменны. Все изменения, происходящие во Вселенной, являются лишь последствием изменения связей между атомами, но не в самих атомах. Таким образом он грамотно обошел споры мыслителей Древней Греции по поводу того, что мир вокруг нас постоянно изменяется.
В начале XIX века начали появляться первые теории химии, до этих пор теория о строении всего вокруг из атомов оставалась лишь философским предположением. Химики первыми обнаружили, что вещество во время химической реакции может распадаться на другие компоненты. Вода, к примеру, распадается на кислород и водород, которые в свою очередь уже не распадутся на более простые частицы, так как они являются элементарными. Такие вещества были названы химическими элементами.
В начале XIX века были открыты примерно тридцать химических элементов. Ученые еще в то время установили, что во время химической реакции количество элементов не меняется. К примеру, для получения воды нужны одна массовая часть водорода и восемь массовых частей кислорода.
Теория атома Бора
Бор выдвинул постулаты, позволяющие рассчитывать спектр атомов водорода и систем, подобных ему, то есть систем, которые состоят из ядра з зарядом Ze и одного электрона (к примеру, ионы He+, Li+). Согласно теории Бора, можно определить несколько физических величин:
- радиус стационарных орбит: \(r_n = < \over >∙n^2, \) \(r_1=52,8 пм;\)
- энергия электрона на стационарной орбите: \(E_n =-13,6< Z^2 \over n^2>; \)
- скорость электрона на орбите: \(v =< Ze^2 \over 4πε_0 t_1 n>. \) .
На вращающийся по орбите электрон действует кулоновская сила взаимодействия с ядром и центробежная сила.
Не нашли что искали?
Просто напиши и мы поможем
Нужна помощьТеория атома Дальтона
Английский химик Д. Дальтон был первым, кто добился существенных результатов в атомистическом развитии химии. В начале XIX века он открывает и формулирует ряд законов: парциальных давлений, о растворимости газов в жидкостях, кратных отношений.
Основные тезисы теории Дальтона звучат таким образом:
- все вещества состоят из огромного количества атомов, которые являются мельчайшими неделимыми и неразрушимыми частицами;
- все атомы одного вещества идентичны по весу и по химическим свойствам. Отличаются лишь атомы различных веществ;
- атомы различных элементов могут соединяться между собой в определенных соотношениях;
- во время химических реакций атомы не могут исчезнуть или измениться, одним из самых важных их свойств есть атомный вес.
В 1803 году Дальтон создал таблицу, которая содержала относительные веса атомов некоторых элементов и соединений, при этом за основу было принято равенство атомного веса водорода единице. Подобного рода таблица была первой. Для того, чтобы обозначить атомы элементов, Дальтон впервые применил условное обозначение в виде круга с изображением различных фигур внутри него. Позже ученый многократно корректировал атомные веса многих элементов, ведь по началу он неверно определял их веса.
Дальтон допустил, что атомы химических элементов во время образования различных сложных атомов соединяются по принципу наибольшей простоты, а именно:
- если есть лишь одно бинарное соединение двух элементов, то его молекула (сложный атом) будет образовываться при помощи одного атома одного элемента и одного атома другого элемента. В соответствии с терминологией Дальтона сложный атом называется двойной;
- если есть два и более соединений, состоящих из двух элементов, то образовавшиеся сложные атомы будут тройные или более.
Соответственно, Дальтон определил, что молекула воды состоит из одного атома кислорода и двух атомов водорода. Исходя из этого, он занизил важность атомного веса кислорода, и впоследствии ложно определил атомные веса металлов, входящих в оксиды.
Вследствие этого принцип максимальной простоты, который применил Дальтон, оказался ложным и отрицательно воздействовал на дальнейшее развитие теории атомных весов. Но, невзирая на это, его теория атома послужила основой для дальнейшего развития химии.
Сложно разобраться самому?
Попробуй обратиться за помощью к преподавателям
Планетарная модель атома Резерфорда
Исследования в области изучения атомов продолжил ученый Э. Резерфорд в 1911 году. В ходе своих экспериментов, исследуя поведение альфа-частиц, он обнаружил, что в атоме присутствуют определенные положительно заряженные частицы. Резерфорд определил, что при прохождении лучей сквозь газ, некоторое число частиц отклоняется от общего направления движения (они практически разворачивались на 180 градусов).
Ученый сделал вывод, что подобное поведение объясняется фактом столкновения этих частиц с положительно заряженными. Эти исследования привели к появлению модели строения атома Резерфорда.
Благодаря своим опытам, Резерфорд создал существенно новую теорию в области изучения атомов. Открытия этого ученого имели огромное значение в последующем развитии важнейшей науки - физики. Модель Резерфорда представляет собой атом в форме ядра, которое расположено в центре, и вращающихся вокруг него электронов. Ядро положительно заряжено, а электроны - отрицательно. Эта модель подобна планетной системе, в которой планеты движутся по орбитам вокруг Солнца, здесь же вокруг ядра по орбитам движутся электроны. Поэтому данная модель получила название планетарной.
Это открытие объяснило причину отклонения альфа-частиц и послужило серьёзным подспорьем в области дальнейшего развития ядерной физики.
Читайте также:

